Cantargia: ESMO 2023-presentation av kliniska fas I-interimsdata för nadunolimab i trippelnegativ bröstcancer visar lovande effekt och säkerhet
Cantargia (Cantargia AB; Nasdaq Stockholm: CANTA) presenterade idag positiva effektsignaler och god säkerhet från fas Ib av den kliniska studien TRIFOUR som undersöker den IL1RAP-bindande antikroppen nadunolimab (CAN04) i metastaserande trippelnegativ bröstcancer (TNBC). Nadunolimab i kombination med cellgifter visade en responsfrekvens på 60% och PFS på 6,6 månader i median i de 15 inkluderade patienterna, vilket är väsentligt högre än historiska kontrolldata. Kombinationen tolererades väl med en säkerhetsprofil liknande den för enbart cellgifter. Datan presenteras idag på en postersession på ESMO 2023 i Madrid. Den randomiserade fas II-delen av TRIFOUR pågår.
“Detta nya dataset i metastaserande trippelnegativ bröstcancer är mycket spännande och den pågående randomiserade fas II-delen i studien är ett logiskt nästa steg. Vi är oerhört motiverade att fortsätta vårt samarbete med GEICAM i denna studie, med målet att utveckla nya behandlingsalternativ för denna svårbehandlade sjukdom,” säger Göran Forsberg, VD på Cantargia.
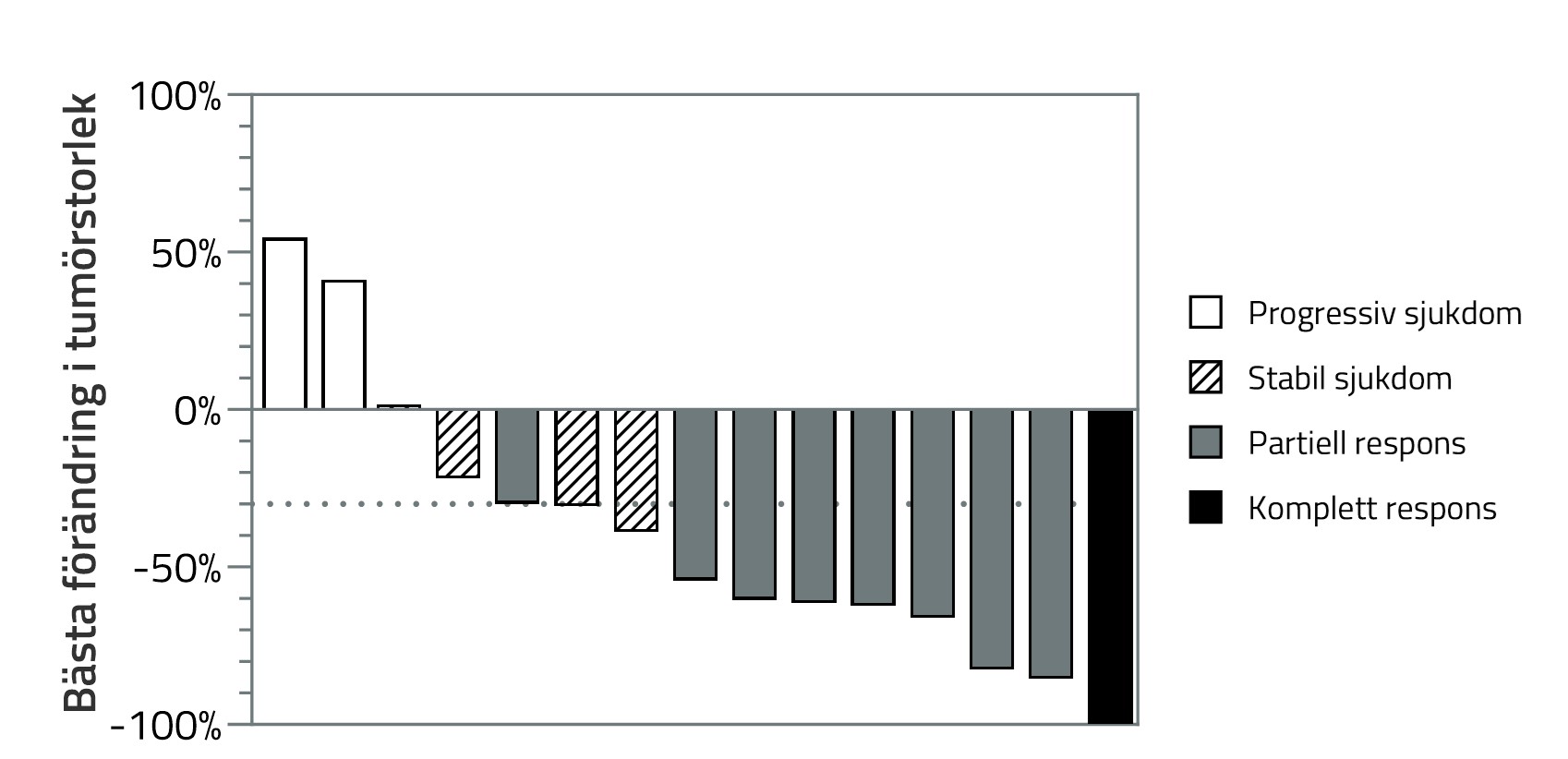
I doseskaleringsdelen av fas Ib/II-studien TRIFOUR, behandlades patienter med metastaserande TNBC, fem i första linjen och tio i andra linjen, med nadunolimab i kombination med gemcitabin och carboplatin. En interimsanalys för dessa 15 patienter visar en bekräftad komplett respons (CR) och åtta bekräftade partiella responser (PR), vilket motsvarar en total preliminär responsfrekvens (RR) på 60%. För närvarande är progressionsfri medianöverlevnad (PFS) 6,6 månader och en tidig uppskattning av total medianöverlevnad (OS) är 12,3 månader. Detta är en förbättring mot historiska data för enbart gemcitabin och carboplatin som visar 30% RR, 4,1 månader PFS i median och 11,1 månader OS i median [1]. Den rekommenderade fas II-dosen av nadunolimab var 2,5 mg/kg som nu utvärderas i den pågående fas II-delen i studien.
Säkerhetsprofilen för kombinationen liknar tidigare resultat för enbart cellgifter. De vanligaste biverkningarna av grad 3 eller 4 var neutropeni (53%) och trombocytopeni (27%), vilket är i likhet med tidigare studier för enbart denna cellgiftsregim (53% respektive 24%) [1]. Som en del av studieprotokollet gavs profylaktisk behandling med G-CSF för att hantera neutropeni.
TRIFOUR, som görs i samarbete med den spanska bröstcancerorganisationen GEICAM, gick vidare in i den randomiserade fas II-delen under Q1 2023. Baserat på de lovande fas Ib-data som presenteras idag, och då inga ytterligare säkerhetssignaler registrerats i fas II-delen, kommer en ändring i studieprotokollet lämnas in för att möjliggöra fullrekrytering till TRIFOUR utan en interimsanalys för futilitet. Denna ändring kräver godkännande av den regulatoriska och etiska kommittén. En top line-analys för hela studien planeras efter fullrekrytering och förväntas sent 2024 eller tidigt 2025.
”Trippelnegativ bröstcancer har sämst prognos av alla bröstcancertyper och har mycket begränsade behandlingsalternativ. Datan som presenteras idag indikerar en lovande tidig effektsignal, som vi är väldigt angelägna om att utvärdera ytterligare i den randomiserade delen av TRIFOUR,” säger Dr. Sara López-Tarruella, medlem i GEICAM:s styrgrupp, koordinator för GEICAM:s arbetsgrupp för trippelnegativ bröstcancer, och en av studieledarna för TRIFOUR-studien.
Mer information om postersessionen på ESMO 2023 anges nedan. Postern är även tillgänglig på Cantargias hemsida (länk). Ett posterabstract baserat på en tidigare avläsning presenterades 16 oktober 2023.
Abstrakttitel: Phase Ib safety and efficacy of nadunolimab/gemcitabine/carboplatin (NadGC) in metastatic triple negative breast cancer (mTNBC)
Datum och tid: 21 oktober 2023, 12:00 – 13:00 CEST
Presentatör: Dr. Sara López-Tarruella
Referenser
[1] O’Shaughnessy, J Clin Oncol 2014, 32:3840-3847

